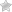Наименьшая частичка любого вещества называется молекулой. Она, в свою очередь, состоит из атомов химических элементов.
Все молекулы определенного вещества имеют одинаковое строение. Наиболее сложное — у молекул органических веществ. Они могут состоять из десятков тысяч атомов.
Молекулы воды
Основные органические вещества, участвующие в жизни любого организма, — это белки, жиры и углеводы.
Белки служат строительным материалом, играют защитную роль, ускоряют химические реакции в организме, переносят кислород. Углеводы являются источником энергии. Жиры хранят ее запасы.
Имеются в нашем теле и другие органические соединения. Из них состоит почти третья часть нашего организма.
Молекула белка
Основой живой материи являются биологические молекулы — нуклеиновые кислоты и белки. Последние представляют собой молекулы-цепочки, состоящие из множества аминокислот (эти кислоты названы так потому, что в них содержатся аминогруппы, состоящие из одного атома азота и двух атомов водорода).
Порядок, в котором располагаются аминокислоты в белке, зашифрован в нуклеиновых кислотах. А участок ДНК, кодирующий один белок, носит название ген. Нуклеиновые кислоты реплицируются, то есть копируются.
Благодаря этому наследственная информация передается от клетки к клетке при делении и от родителей детям.
Молекула органического вещества
Нуклеиновые кислоты бывают двух основных типов — дезоксирибонуклеиновая кислота (ДНК) и рибонуклеиновая кислота (РНК). Полимерная молекула ДНК состоит из отдельных звеньев — мономеров, или нуклеотидов.
Каждый нуклеотид — это сахар (дезоксирибоза), остаток фосфорной кислоты и одно из четырех азотистых оснований — аденин, гуанин, цитозин, тимин. Азотистые основания связываются друг с другом по принципу тимином, а гуанин — с цитозином. Так образуется двойная спираль ДНК.
Молекула РНК обычно состоит из одной цепочки; вместо дезоксирибозы в ней имеется рибоза, а вместо тимина — урацил.
Две молекулы — ДНК и РНК — носители генетической информации
Хромосомы — структуры в ядре клетки, состоящие из ДНК и белка. Именно в хромосомах сосредоточена большая часть наследственной информации. Набор всех хромосом клетки называется кариотипом.
У каждого вида свое определенное количество хромосом. У гориллы их 48, у лошади — 64, у одного из видов муравьев — 2, а у простейшего животного радиолярии — 1600.
Так что уровень развития не зависит от числа хромосом.
ДНК, расположенные особым образом с некоторыми белками, составляют хромосомы. Практически все хромосомы находятся в ядре клетки. Исключение составляет митохондриальная ДНК, которая находится в цитоплазме
У человека 46 хромосом (23 пары). 22 пары называются аутосомами, а одна пара — половыми хромосомами. У женщин половые хромосомы, или Х-хромосомы, одинаковы. У мужчин есть одна Х-хромосома и одна У-хромосома. Поэтому правильный кариотип женщины обозначается формулой 46ХХ, а кариотип мужчины — 46ХУ.
Синтез белка и генетический код
Синтез белка состоит из трех этапов — транскрипции, процессинга и трансляции. Во время транскрипции, или считывания, на одной из цепочек ДНК синтезируется молекула РНК.
Созревая во время процессинга, она выходит из ядра в цитоплазму, где на особых структурах — рибосомах — синтезируется полипетидная цепь, то есть цепочка связанных между собой аминокислот.
Их последовательность определяется последовательностью нуклеотидов, составляющих ДНК и РНК, то есть генетическим кодом.
Генетический код — система записи генетической информации, согласно которой каждому кодону, представляющему собой последовательность из трех нуклеотидов, соответствует аминокислота. Причем у одной аминокислоты бывает несколько кодонов.
Существуют также стартовый и стоп-кодоны, которые определяют начало и окончание синтеза. Если происходит мутация, то есть один нуклеотид заменяется на другой либо один или несколько нуклеотидов добавляются в цепочку или удаляются, кодоны меняются. И вместо одной аминокислоты кодируется другая.
А значит, меняется состав белка и, скорее всего, его свойства. Такие изменения называются мутациями.
Генетический код един для всей живой природы нашей планеты. Совокупность генов конкретного организма — это генотип. А геном — совокупность генетического материала в гаплоидном наборе хромосом конкретного вида. Поэтому следует говорить: геном человека или собаки, генотип Ивана Ивановича или овчарки Рекса, генетический код всего живого. А вот фенотип — это совокупность всех признаков организма, гены при этом проявляются далеко не все.
Из 22 аминокислот синтезируются самые разные белки. Например, у цепочки из 100 аминокислотных остатков может существовать более 10 130 вариантов белков с разной последовательностью. При этом белки имеют первичную, вторичную, третичную и четвертичную структуры. Все зависит от того, как скручивается первоначальная цепочка.
Удивительно, но в живой природе для построения всего многообразия белков используется лишь 22 аминокислоты. Одни аминокислоты могут создаваться в самом организме, другие поступают в него с пищей, они называются незаменимыми.
Особой группой белков являются ферменты. Эти вещества ускоряют превращение веществ, поступающих в организм с пищей, в молекулы, нужные для организма. Ферменты присутствуют во всех живых клетках и принимают активное участие в обмене веществ и энергии. Без ферментов живой организм существовать просто не может.
А у каждого фермента, состоящего из сложных молекул, есть так называемый активный центр — углубление особой формы, которое должно соответствовать определенному веществу наподобие ключа в замке. Это соответствие должно быть абсолютным. Поэтому каждый фермент взаимодействует только с определенным веществом. На сегодня известно более 2000 ферментов, но ни один из них нельзя заменить другим.
Множество ферментов участвует и в обмене веществ внутри клетки.
Благодаря ферментам скорость расщепления веществ, полученных с пищей, увеличивается в миллионы раз.
Как увидеть ДНК и хромосомы?
Изучение структуры ДНК раскроет историю развития живой природы и поможет победить многие болезни.
Молекула ДНК, если ее специально выделить из клеток крови или другой ткани, видна невооруженным глазом как белая нить, иногда спутанная и скрученная, или белое полупрозрачное вещество, похожее на медузу.
Но для того чтобы различить ее структуру, нужны специальные приборы. А хромосомы можно разглядеть в обычный микроскоп.
Изучение структуры ДНК раскроет историю развития всей живой природы и поможет победить многие болезни.
Что умеют делать белки?
Белки выполняют множество самых разнообразных задач. Одни из них являются источниками питания для потомства. Например, белок яйца или белок молока.
Защиту организма от бактерий и вирусов выполняют антитела крови, которые также состоят из белков. Связываясь с чужеродными веществами, антитела нейтрализуют их и таким образом охраняют организм.
Белки участвуют в переносе нужных веществ к органам и обеспечивают тончайшие процессы жизнедеятельности самих клеток.
Что такое жиры?
Жиры — это органические вещества, возникающие в результате изменения (этерификации) карбоновых кислот и трехатомного спирта глицерина.
Они присутствуют в каждом живом организме, входя в состав клеточной мембраны. При их окислении образуется большое количество необходимой телу энергии.
Жиры могут получаться из углеводов и белков и накапливаться в организме. Затем, при недостатке пищи, они расходуются.
Высокое содержание жиров в семенах растений обеспечивает развитие зародышей до их перехода к самостоятельному питанию.
Продукты, содержащие жиры
Жировой слой в подкожной клетчатке животных защищает организм от механических повреждений. Он помогает телу сохранить тепло, что позволяет многим животным жить в условиях холодного климата. А у китов жир способствует их плавучести.
Тонким слоем жира покрыты кожа, шерсть и перья многих животных. Он делает их более эластичными и предохраняет от влаги. Жировой пленкой покрыты листья и плоды многих растений. В нервных клетках жиры являются изоляторами при проведении нервных импульсов. Жиры используются пчелами для изготовления воска при строительстве сот.
Из жиров при окислении может получаться вода. Так, 100 г жира дает примерно 105 г воды. Это свойство очень важно для некоторых жителей жарких пустынь, например для верблюдов, способных обходиться без воды в течение 10—12 суток. Жир, накопленный в их горбах, используется именно для получения воды.
Животные, впадающие в спячку (медведи, сурки и другие), способны обходиться без воды и пищи по несколько месяцев. Это они могут делать благодаря накопленному жиру, из которого организм получает необходимую энергию и воду. Так, за время спячки животные могут терять почти половину своего веса.
Что такое углеводы?
Модель молекулы сахарозы. Белым цветом здесь обозначены атомы водорода, черным углерода, красным — кислорода
Углеводы — общее название обширной группы органических веществ. Свое название они получили от слов «углерод» и «вода», поскольку первые известные углеводы представлялись как химическое соединение углерода и воды.
В живой природе углеводы «изготавливаются» растениями, а животные и человек получают их с пищей. Большую группу углеводов называют сахарами.
Известный нам сахар — это тоже углевод, научное название которого — сахароза.
Углеводы являются основным источником энергии, получаемой организмом. Они используются и для построения многих сложных молекул, важных для живых существ. У растений из углеводов построены прочные стенки клеток.
Продукты, в которых имеется углерод
Углеводы также могут превращаться в жиры и накапливаться как запасы питательных веществ.
Для чего нужны пища, вода и кислород?
Все живые организмы не могут жить без пищи, которая необходима им для получения энергии и строительства своего тела. Все необходимое они берут из окружающей среды. При этом каждый организм является пищей для какого-либо другого.
Молекула кислорода состоит из двух атомов кислорода, а молекула озона, который защищает
Основными материалами, которые организм получает с пищей, являются белки, жиры, углеводы, вода, кислород и углекислый газ. В клетках организма эти вещества перерабатываются и превращаются в материалы, нужные для жизни. Лишние детали они отдают во внешнюю среду.
Таким образом, в любом живом организме одновременно происходят и строительство (анаболизм), и распад (катаболизм) веществ, что сопровождается поглощением или выделением энергии.
Этот процесс называется обменом веществ.
Тело человека на две трети состоит из воды, а во многих растениях ее содержится более 80%. Каждый день организм человека теряет большое количество воды с выводимой мочой, потом и выдыхаемым воздухом.
Поэтому человек должен восполнять потери воды, например, в процессе питья или получая ее с пищей. Некоторое количество воды образуется при расщеплении жиров.
Суточная потребность человека в воде составляет около 3 л.
Больше всего живым организмам необходима вода. Без нее жизнь на нашей планете была бы невозможной. Она является важнейшим веществом всех видов клеток, межклеточной жидкости и крови. Вода — растворитель многих солей и органических соединений. А водные растворы лучше всего усваиваются всеми органами.
Газообмен в человеческом организме
Практически вся жизнь на Земле зависит от кислорода. Он все время нужен каждой клеточке животного или растения. Ведь с его помощью внутри клетки различные органические вещества разлагаются на более простые. Этот процесс называют окислением.
При этом выделяется энергия, необходимая для роста и жизнедеятельности клеток. Наверняка каждый человек хоть однажды наблюдал, как горят дрова в костре. Горение — это тоже окисление. То же самое происходит в организме, только гораздо медленнее.
Кислород
Не будет кислорода — не будет энергии в клетке, и ее жизнь прекратится. Это приведет к гибели всего организма. Без пищи живые существа могут существовать в течение 1-2 недель, без воды — 5-6 дней. Но без достаточного количества кислорода они не смогут прожить и нескольких минут.
Вопросы для самопроверки
- Из чего состоят белки?
- Чем ДНК отличается от РНК?
- Зависит ли от количества хромосом уровень развития?
- На чем и с помощью чего синтезируется белок?
- Чем отличается генетический код от генотипа?
- Что делают ферменты?
- Какую еще роль кроме запасания энергии играет жир в клетке?
- Во что могут превращаться углеводы?
- Что такое обмен веществ?
- Что общего у горения и окисления?
Ответы
- Белки состоят из аминокислот.
- ДНК — двухцепочечная молекула, в ней имеются основания — аденин, тимин, гуанин и цитозин. РНК в основном состоит из одной цепочки, и вместо тимина в ней имеется урацил.
- Уровень развития от количества хромосом не зависит.
Например, у простейшей радиолярии 1600 хромосом, у гораздо более «продвинутого» муравья — 2, у обезьяны — 48, а у человека — 46.
- Белок синтезируется с помощью молекул ДНК и РНК на рибосомах.
- Генетический код — это система записи генетической информации, а генотип — совокупность генов конкретного организма.
- Ферменты ускоряют биохимические реакции в организме.
- Молекулы жиров входят в состав клеточной мембраны.
- Углеводы могут превращаться в жиры.
- Обмен веществ — это набор химических реакций, в процессе которых сложные вещества распадаются до более простых, а из простых синтезируются другие сложные вещества, необходимые организму.
- Горение — это быстрое окисление.
Поделиться ссылкой
Простые и сложные вещества Звонарёва Т.И. Учитель биологии МОУ лицей Г. Электрогорск – скачать презентацию
Слайд 1Описание слайда:
Простые и сложные вещества Звонарёва Т.И. Учитель биологии МОУ лицей Г. Электрогорск
Слайд 2Описание слайда:
Допиши предложение 1.Тела состоят из … 2. Мельчайшая частица вещества, сохраняющая его свойства это – … 3.Молекулы состоят из … 4. Определённый вид атомов называется … 5. . Молекулы одного и того же вещества …
Слайд 3Описание слайда:
Проверь 1. Веществ 2. Молекула 3. Атомов 4. Химическим элементом 5. Одинаковы
Слайд 4Описание слайда:
Нарисуй схему Молекулу воды Молекулу кислорода Молекулу озона
Слайд 5Описание слайда:
Разнообразие веществ Вещество состоящее из атомов одного вида называется простым
Слайд 6Описание слайда:
вещества, состоящие из атомов одного вида. вещества, состоящие из атомов одного вида. О2 О + О
Слайд 7Описание слайда:
Простые вещества
Слайд 8Описание слайда:
Разнообразие веществ Вещество состоящее из разных видов атомов называется сложным
Слайд 9Описание слайда:
– вещества, состоящие из атомов разных элементов – вещества, состоящие из атомов разных элементов
Слайд 10Описание слайда:
Сложные вещества
Слайд 11Описание слайда:
Простые и сложные вещества
Слайд 12Описание слайда:
Под какими буквами на схемах обозначены простые вещества: Под какими буквами на схемах обозначены простые вещества: О2 СО2 N2 А Б В Г Д Е
Слайд 13Слайд 14Описание слайда:
Угадайте загадки: Меня не едят – И без меня мало едят.
Слайд 15Описание слайда:
Неорганические вещества
Слайд 16Описание слайда:
Органические вещества
Слайд 17Описание слайда:
Разделите перечисленные названия веществ на 2 группы: неорганические вещества и органические: Разделите перечисленные названия веществ на 2 группы: неорганические вещества и органические: Вода, кислород, жиры, медь, водород, белки, поваренная соль, углеводы.
Слайд 18Описание слайда:
К уксусной кислоте прикасаться опасно!
Слайд 19Описание слайда:
Домашнее задание: Учебник с. 55-57 Вопросы:1,2
Простые и сложные вещества
- Простые вещества: молекулы состоят из атомов одного вида (атомов одного элемента).
- Пример: H2, O2,Cl2, P4, Na, Cu, Au.
- Сложные вещества (или химические соединения): молекулы состоят из атомов разного вида (атомов различных химических элементов).
- Пример: H2O, NH3, OF2, H2SO4, MgCl2, K2SO4.
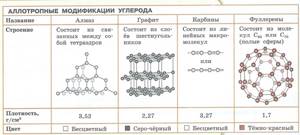
- Аллотропия — способность одного химического элемента образовывать несколько простых веществ, различающихся по строению и свойствам.
- Пример:
- С – алмаз, графит, карбин, фуллерен.
- O – кислород, озон.
- S – ромбическая, моноклинная, пластическая.
- P – белый, красный, чёрный.
Явление аллотропии вызывается двумя причинами:
- Различным числом атомов в молекуле, например кислород O2 и озон O3.
- Образованием различных кристаллических форм, например алмаз, графит, карбин и фуллерен (смотри рисунок выше).
Основные классы неорганических веществ
Бинарные соединения
Вещества, состоящие из двух химических элементов называются бинарными (от лат. би – два) или двухэлементными.
- Названия бинарных соединений образуют из двух слов – названий входящих в их состав химических элементов.
- Первое слово обозначает электроотрицательную часть соединения – неметалл, его латинское название с суффиксом –ид стоит всегда в именительном падеже.
- Второе слово обозначает электроположительную часть – металл или менее электроотрицательный элемент, его название стоит в родительном падеже, затем указывается степень окисления (только в том случае, если она переменная):
Запомни!
- BH3 — боран
- B2H6 — диборан
- CH4 — метан
- SiH4 — силан
- NH3 — аммиак
- PH3 — фосфин
- AsH3 — арсин
Оксиды
Оксиды — сложные вещества, состоящие из двух химических элементов, один из которых кислород в степени окисления -2.
Общая формула оксидов: ЭхОу
Основные оксиды
Основные оксиды — оксиды, которым соответствуют основания.
Основные оксиды образованы металлом со степенью окисления +1, +2.
Пример
Соответствие основных оксидов и оснований
- Na2O — Na2(+1)O(-2) — NaOH
- MgO — Mg(+2)O(-2) — Mg(OH)2
- FeO — Fe(+2)O(-2) — Fe(OH)2
- MnO — Mn(+2)O(-2) — Mn(OH)2
Амфотерные оксиды
Амфотерные оксиды — оксиды, которые в зависимости от условий проявляют либо основные, либо кислотные свойства.
Амфотерные оксиды образованы металлом со степенью окисления +3, +4, а также некоторыми металлами (Zn, Be) со степенью окисления +2.
Пример
Al2(+3)O3(-2), Fe2(+3)O3(-2), Mn(+4)O2(-2), Zn(+2)O(-2), Be(+2)O(-2)
Кислотные оксиды
Кислотные оксиды — оксиды, которым соответствуют кислоты.
Кислотные оксиды образованы неметаллом, а также металлом со степенью окисления +5, +6, +7.
Пример
Соответствие кислотных оксидов и кислот
- SO3 — S(+6)O3(-2) — H2SO4
- N2O5 — N2(+5)O5(-2) — HNO3
- CrO3 — Cr(+6)O3(-2) — H2CrO4
- Mn2O7 — Mn2(+7)O7(-2) — HMnO4
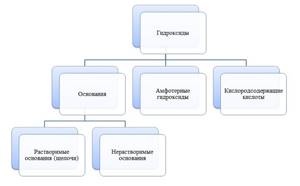
Гидроксиды
Гидроксиды — сложные вещества, состоящие из трех элементов, два из которых водород со степенью окисления +1 и кислород со степенью окисления -2.
Общая формула гидроксидов: ЭхОуНz
Основания
Основания — сложные вещества, состоящие из ионов металла и одной или нескольких гидроксо-групп (ОН-).
В основаниях металл имеет степень окисления +1, +2 или вместо металла стоит ион аммония NH4+
Пример
NaOH, NH4OH, Ca(OH)2
Амфотерные гидроксиды
Амфотерные гидроксиды — сложные вещества, которые в зависимости от условий проявляют свойства оснований или кислот.
Амфотерные гидроксиды имеют металл со степенью окисления +3, +4, а также некоторые металлы (Zn, Be) со степенью окисления +2.
Пример
Zn(OH)2, Be(OH)2, Al(OH)3, Cr(OH)3
Кислоты
Кислоты — сложные вещества, состоящие из атомов водорода и кислотных остатков.
В состав кислот входит неметалл или металл со степенью окисления +5, +6, +7.
Пример
H2SO4, HNO3, H2Cr2O7, HMnO4
Соли
Соли- соединения, состоящие из катионов металлов (или NH4+) и кислотных остатков.
Общая формула солей: MexAcy
- Me – металл
- Ac – кислотный остаток
Пример
- KNO3 — нитрат калия
- (NH4)2SO4 — сульфат аммония
- Mg(NO3)2 — нитрат магния
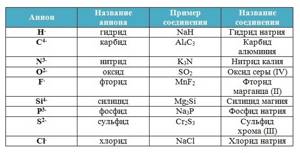
Названия кислот и кислотных остатков
| Кислота | Кислотный остаток | ||
| Название | Формула | Название | Формула |
| Соляная (хлороводородная) | HCl | Хлорид | Cl(-) |
| Плавиковая (фтороводородная) | HF | Фторид | F(-) |
| Бромоводородная | HBr | Бромид | Br(-) |
| Иодоводородная | HI | Иодид | I(-) |
| Азотистая | HNO2 | Нитрит | NO2(-) |
| Азотная | HNO3 | Нитрат | NO3(-) |
| Сероводородная | H2S | Сульфид Гидросульфид | S(2-) HS(-) |
| Сернистая | H2SO3 | Сульфит Гидросульфит | SO3(2-) HSO3(-) |
| Серная | H2SO4 | Сульфат Гидросульфат | SO4(2-) HSO4(-) |
| Угольная | H2CO3 | Карбонат Гидрокарбонат | СО3(2-) НСО3(-) |
| Кремниевая | H2SiO3 | Силикат | SiO3(2-) |
| Ортофосфорная | H3PO4 | Ортофосфат ГидроортофосфатДигидроортофосфат | РО4(3-) НРО4(2-) Н2РО4(-) |
| Муравьиная | НСООН | Формиат | НСОО(-) |
| Уксусная | СН3СООН | Ацетат | СН3СОО(-) |
Полезные ссылки
- Источник материала
- Классификация неорганических веществ (видео)
- Классификация неорганических веществ. Сложные вопросы (видео)
- Кислотные оксиды (видео)
- Основные оксиды (видео)
- Основания (видео)
- Характеристика солей (видео)
Дополнительные материалы
- Классификация и номенклатура неорганических веществ (видео)
- Классификация соединений (видео)
- Аллотропные формы углерода (видео)
§ 1.5. Простые и сложные вещества. Аллотропы. Химические вещества и смеси
В предыдущей главе было сказано, что образовывать связи друг с другом могут не только атомы одного химического элемента, но также атомы разных элементов.
Вещества, образованные атомами одного химического элемента, называют простыми веществами, а вещества, образованные атомами разных химических элементов, — сложными. Некоторые простые вещества имеют молекулярное строение, т.е. состоят из молекул.
Например, молекулярное строение имеют такие вещества, как кислород, азот, водород, фтор, хлор, бром, йод. Каждое из этих веществ образовано двухатомными молекулами, поэтому их формулы можно записать как O2, N2, H2, F2, Cl2, Br2 и I2 соответственно.
Как можно заметить, простые вещества могут иметь одинаковое название с элементами, их образующими. Поэтому следует четко различать ситуации, когда речь идет о химическом элементе, а когда о простом веществе.
Нередко простые вещества имеют не молекулярное, а атомное строение. В таких веществах атомы могут образовывать друг с другом связи различных типов, которые подробно будут рассмотрены чуть позже. Веществами подобного строения являются все металлы, например, железо, медь, никель, а также некоторые неметаллы — алмаз, кремний, графит и т.д.
Для данных веществ обычно характерно не только совпадение названия химического элемента с названием им образованного вещества, но также идентичны запись формулы вещества и обозначения химического элемента.
Например, химические элементы железо, медь и кремний, имеющие обозначения Fe, Cu и Si, образуют простые вещества, формулы которых Fe, Cu и Si соответственно. Существует также небольшая группа простых веществ, состоящих из разрозненных атомов, никак не связанных между собой.
Такие вещества являются газами, которые называют, ввиду их крайне низкой химической активности, благородными. К ним относятся гелий (Не), неон (Ne), аргон (Аr), криптон (Кr), ксенон (Хе), радон (Rn).
Поскольку только известных простых веществ насчитывается около 500, то логично вытекает вывод о том, что для многих химических элементов характерно явление, называемое аллотропией.
Аллотропия – явление, когда один химический элемент может образовывать несколько простых веществ. Разные химические вещества, образованные одним химическим элементом, называют аллотропными модификациями или аллотропами.
Так, например, химический элемент кислород может образовывать два простых вещества, одно и которых имеет название химического элемента – кислород. Кислород как вещество состоит из двухатомных молекул, т.е. формула его O2.
Именно данное соединение входит в состав жизненно необходимого нам воздуха. Другой аллотропной модификацией кислорода является трехатомный газ озон, формула которого O3.
Несмотря на то что и озон, и кислород образованы одним химическим элементом, их химическое поведение весьма различно: озон отличается намного большей активностью по сравнению с кислородом в реакциях с теми же веществами.
Кроме того, данные вещества отличаются друг от друга по физическим свойствам уже как минимум из-за того, что молекулярная масса озона больше, чем у кислорода в 1,5 раза. Это приводит к тому, что его плотность в газообразном состоянии также больше в 1,5 раза.
Многие химические элементы склонны образовывать аллотропные модификации, отличающиеся друг от друга особенностями строения кристаллической решетки. Так, например, на рисунке 5, вы можете видеть схематичные изображения фрагментов кристаллических решеток алмаза и графита, которые являются аллотропными модификациями углерода.
Рисунок 5. Фрагменты кристаллических решеток алмаза (а) и графита (б)
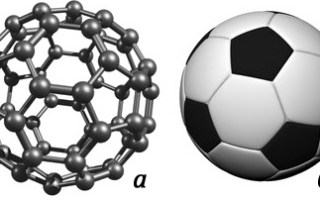
Кроме того, углерод может иметь и молекулярное строение: такая структура наблюдается у такого типа веществ, как фуллерены. Вещества данного типа образованы молекулами углерода сферической формы. На рисунке 6 представлены 3D модели молекулы фуллерена с60 и футбольного мяча для сравнения. Обратите внимание на их интересное сходство.
Рисунок 6. Молекула фуллерена С60 (а) и футбольный мяч (б)
Сложные вещества — это вещества, которые состоят из атомов разных элементов. Они так же, как и простые вещества, могут иметь молекулярное и немолекулярное строение. Немолекулярный тип строения сложных веществ может быть более разнообразен, нежели у простых.
Любые сложные химические вещества могут быть получены либо прямым взаимодействием простых веществ, либо последовательностью их взаимодействий друг с другом.
Важно осознавать один факт, который заключается в том, что свойства сложных вещества как физические, так и химические сильно отличаются от свойств простых веществ, из которых они получены.
Например, поваренная соль, имеющая форуму NaCl и представляющая собой бесцветные прозрачные кристаллы, может быть получена взаимодействием натрия, являющегося металлом с характерными для металлов свойствами (блеск и электропроводность), с хлором Cl2 — газом желто-зеленого цвета.
Серная кислота H2SO4 может быть образована серией последовательных превращений из простых веществ — водорода H2, серы S и кислорода O2.
Водород — газ легче воздуха, образующий с воздухом взрывчатые смеси, сера — твердое вещество желтого цвета, способное гореть, и кислород — газ чуть тяжелее воздуха, в котором могут гореть многие вещества.
Серная кислота, которая может быть получена из данных простых веществ, представляет собой тяжелую маслянистую жидкость, обладающая сильными водоотнимающими свойствами, из-за которых обугливает многие вещества органического происхождения.
Очевидно, что помимо индивидуальных химических веществ, бывают также и их смеси. Преимущественно именно смесями различных веществ образован мир вокруг нас: сплавы металлов, продукты питания, напитки, различные материалы, из которых состоят окружающие нас предметы.
Например, воздух, которым мы дышим, состоит в основном из азота N2 (78%), жизненно необходимого нам кислорода (21%), оставшийся же 1% приходится на примеси других газов (углекислый газ, благородные газы и др.).
Смеси веществ разделяют на гомогенные и гетерогенные. Гомогенными смесями называют такие смеси, у которых нет границ раздела фаз.
Гомогенными смесями являются смесь спирта и воды, сплавы металлов, раствор соли и сахара в воде, смеси газов и т.д. Гетерогенными смесями называют такие смеси, у которых имеется граница раздела фаз.
К смесям такого типа можно отнести смесь песка и воды, сахара и соли, смесь масла и воды и др.
Вещества, из которых состоят смеси, называют компонентами.
Смеси простых веществ в отличие от химических соединений, которые могут быть получены из этих простых веществ, сохраняют свойства каждого компонента.
Вопросы к параграфу 8 – ГДЗ по Биологии 5 класс Учебник Пасечник (решебник)
Издательство: Просвещение/Дрофа
Химический элемент — это определенный вид атомов. Атомы разных химических элементов отличаются массой, размерами, строением и свойствами. На данный момент известно более 118 химических элементов (азот, углерод, кислород, кальций, магний и др.)
2. Какие органические вещества вам известны?
Органические вещества входят в состав всех живых организмов. К ним относят углеводы, белки, жиры, нуклеиновые кислоты и другие вещества.
3. Какие вещества называют простыми, а какие — сложными?
Простыми химическими веществами называют вещества, которые состоят из атомов только одного химического элемента (углерод, железо, азот, кислород)
К сложным химическим элементам относятся вещества, состоящие из атомов двух и более химических элементов (вода, уксус, углекислый газ).
Вопросы в конце параграфа
1. Каких химических элементов больше всего в клетке?
Около 98% от массы любой клетки приходится на четыре элемента: углерод, водород, кислород и азот.
2. Какую роль в клетке играет вода?
Содержание воды в клетке составляет от 40 до 95% её общей массы. Вода придает клетке упругость, определяет её форму, участвует в обмене веществ.
Чем выше интенсивность обмена веществ в той или иной клетке, тем больше в ней содержится воды.
3. Какие вещества относят к органическим?
К органическим веществам относятся углеводы, белки, жиры, нуклеиновые кислоты и другие вещества.
4. Каково значение органических веществ в клетке?
В результате расщепления углеводов клетки получают энергию, необходимую для их жизнедеятельности. Углеводы входят в состав оболочек клеток, придавая им прочность. Питательные вещества, что запасаются в клетках (крахмал и сахара) являются углеводами.
- Белки входят в состав разнообразных клеточных структур, регулируют процессы жизнедеятельности и также могут запасаться в клетках.
- Жиры откладываются в клетках и служат источником энергии (выделяется при расщеплении), необходимой живым организмам.
- Нуклеиновые кислоты нужны для сохранения наследственной информации и передаче её потомкам.
Подумайте
Почему клетку сравнивают с «миниатюрной природной лабораторией»?
Клетку сравнивают с «миниатюрной природной лабораторией», потому что в этой мельчайшей частицы организма происходит много сложных процессов, синтезируются и претерпевают изменения различные химические соединения.
Простые и сложные вещества. Аллотропия. Химические соединения и смеси
Все вещества делятся на простые и сложные.
Простые вещества — это вещества, которые состоят из атомов одного элемента.
В некоторых простых веществах атомы одного элемента соединяются друг с другом и образуют молекулы. Такие простые вещества имеют молекулярное строение. К ним относятся: водород H2, кислород O2, азот N2, фтор F2, хлор Cl2, бром Br2, йод I2. Все эти вещества состоят из двухатомных молекул. (Обратите внимание, что названия простых веществ совпадают с названиями элементов!)
Другие простые вещества имеют атомное строение, т. е. состоят из атомов, между которыми существуют определенные связи. Примерами таких простых веществ являются все металлы (железо Fe, медь Сu, натрий Na и т. д.) и некоторые неметаллы (углерод С, кремний Si и др.). Не только названия, но и формулы этих простых веществ совпадают с символами элементов.
Существует также группа простых веществ, которые называются благородными газами. К ним относятся: гелий Не, неон Ne, аргон Аr, криптон Kr, ксенон Хе, радон Rn. Эти простые вещества состоят из не связанных друг с другом атомов.
Каждый элемент образует как минимум одно простое вещество. Некоторые элементы могут образовывать не одно, а два или несколько простых веществ. Это явление называется аллотропией.
Аллотропия — это явление образования нескольких простых веществ одним элементом.
Разные простые вещества, которые образуются одним и тем же химическим элементом, называются аллотропными видоизменениями (модификациями).
Аллотропные модификации могут отличаться друг от друга составом молекул. Например, элемент кислород образует два простых вещества. Одно из них состоит из двухатомных молекул О2 и имеет такое же название, как и элемент— кислород. Другое простое вещество состоит из трехатомных молекул О3 и имеет собственное название — озон.
Кислород О2 и озон О3 имеют различные физические и химические свойства.
Аллотропные модификации могут представлять собой твердые вещества, которые имеют различное строение кристаллов. Примером являются аллотропные модификации углерода С — алмаз и графит.
Число известных простых веществ (примерно 400) значительно больше, чем число химических элементов, так как многие элементы могут образовывать две или несколько аллотропных модификаций.
Сложные вещества — это вещества, которые состоят из атомов разных элементов.
Примеры сложных веществ: НCl, Н2O, NaCl, СО2, H2SO4 и т. д.
Сложные вещества часто называют химическими соединениями. В химических соединениях свойства простых веществ, из которых образуются эти соединения, не сохраняются. Свойства сложного вещества отличаются от свойств простых веществ, из которых оно образуется.
Например, хлорид натрия NaCl может образоваться из простых веществ — металлического натрия Na и газообразного хлора Сl Физические и химические свойства NaCl отличаются от свойств Na и Cl2.
В природе, как правило, встречаются не чистые вещества, а смеси веществ. В практической деятельности мы также обычно используем смеси веществ. Любая смесь состоит из двух или большего числа веществ, которые называются компонентами смеси.
Например, воздух представляет собой смесь нескольких газообразных веществ: кислорода О2 (21 % по объему), азота N2 (78%), углекислого газа СО2 и др. Смесями являются растворы многих веществ, сплавы некоторых металлов и т. д.
- Смеси веществ бывают гомогенными (однородными) и гетерогенными (неоднородными).
- Гомогенные смеси — это смеси, в которых между компонентами нет поверхности раздела.
- Гомогенными являются смеси газов (в частности, воздух), жидкие растворы (например, раствор сахара в воде).
- Гетерогенные смеси — это смеси, в которых компоненты разделяются поверхностью раздела.
- К гетерогенным относятся смеси твердых веществ (песок + порошок мела), смеси нерастворимых друг в друге жидкостей (вода + масло), смеси жидкостей и нерастворимых в нем твердых веществ (вода + мел).
- Важнейшие отличия смесей от химических соединений:
- В смесях свойства отдельных веществ (компонентов) сохраняются.
- Состав смесей не является постоянным.

 Описание слайда:
Описание слайда: Описание слайда:
Описание слайда: Описание слайда:
Описание слайда: Описание слайда:
Описание слайда: Описание слайда:
Описание слайда: Описание слайда:
Описание слайда: Описание слайда:
Описание слайда: Описание слайда:
Описание слайда: Описание слайда:
Описание слайда: Описание слайда:
Описание слайда: