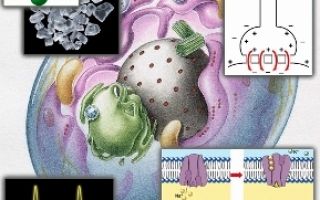
- Неорганические вещества клетки. Минеральные соли
- Минеральные соли могут содержаться в организме в растворенном виде (диссоциированными на ионы) или в нерастворимом виде.
- Важную роль в жизнедеятельности клетки играют растворимые минеральные соли, представленные в основном катионами К+, Na+, Ca2+, Mg2+ и анионами НРО42-, Н2РО4-, Сl-, НСO3-.
Многие ионы неравномерно распределены между клеткой и окружающей средой. Именно благодаря существованию подобных градиентов концентраций осуществляются многие важные процессы жизнедеятельности, такие, например, как возбуждение нервных клеток и сокращение мышечных волокон.
На внешней клеточной мембране высокая концентрация ионов Na+, а на внутренней — ионов К+. Этот факт обуславливает передачу возбуждения по нервам и мышце.
Са2+, Mg2+ являются активаторами многих ферментов, если их недостаточно, то нарушается процесс обмена веществ. Mg2+ поддерживает целостность рибосом, работу митохондрий.
Са3(РО4)2 есть в составе костей, а СаСО3 — в составе раковин моллюсков.
Ионы растворимых солей Na+, K+, Cl- Mg2+, SO42- в организме человека и животных выполняют ряд важных функций:
- создают условия для передачи нервных импульсов;
- регулируют проницаемость мембран;
- участвуют в мышечных сокращениях;
- поддерживают осмотическое давление крови и нормализуют водный баланс;
- регулируют кислотно-щелочной баланс;
- усиливают действие желудочных соков, участвуют в формировании кислых и щелочных ферментов.
Анионы слабых кислот участвуют в поддержании кислотно-щелочного баланса (рН) клетки. Анионы фосфорной кислоты необходимы для синтеза главной энергетической молекулы — АТФ, нуклеотидов и нуклеиновых кислот (ДНК и РНК).
От концентрации солей внутри клетки зависят буферные свойства, то есть способность поддерживать слабощелочную среду. Внутри клетки буферность обеспечивается анионами Н2РО4-, во внеклеточной жидкости и в крови роль буфера играют НРО42-, НСО3-.
Неорганические соли — KNO3, CaSO4, Na3PO4 — служат важными компонентами минерального питания растений.
| Создание осмотического баланса | Состав минеральных солей и их концентрация определяют осмотическое давление жидкостей внутри клеток и полостей тела. Благодаря осмотическому давлению формируется гидроскелет беспозвоночных и тургор растений | Na+, K+, Ca2+, Mg2+, Cl-, HCO3-, H2PO4-, HPO42-, SO42- |
| Поддержание буферных свойств | Буферность — способность поддерживать рН на определенном уровне. За поддержание рН клеток и тканей отвечают фосфатная и бикарбонатная буферные системы | HPO42- + H+ ↔ H2PO4-; HCO3- + H+ ↔ H2CO3 |
| Поддержание градиентов концентраций | В клетке и межклеточном пространстве поддерживаются определенные концентрации ионов. Благодаря существованию градиентов концентраций осуществляются такие важные процессы жизнедеятельности, как возбуждение нервных клеток и сокращение мышечных волокон | Na+, K+, Ca2+, Cl- |
| Формирование скелетных образований | Кости скелета позвоночных в основном состоят из фосфатов кальция и магния. Раковины моллюсков формируются из карбоната кальция | Ca2+, Mg2+, PO43-, CO32- |
| Передача нервных импульсов | Участвуют в работе химических синапсов | Ca2+, К+, Na+, Cl- |
Минеральные вещества в зависимости от их содержания в организме и пищевых продуктах подразделяют на макро- и микроэлементы.
Минеральные или неорганические вещества относят к числу незаменимых, они участвуют в жизненно важных процессах, протекающих в организме человека: построении костей, поддержании кислотно-щелочного равновесия, состава крови, нормализации водно-солевого обмена, в деятельности нервной системы.
В зависимости от содержания в организме минеральные вещества делят на макроэлементы, находящиеся в значительном количестве, микро- и ультрамикроэлименты, входящие в состав тела человека в малых дозах – от тысячных до десятитысячных долей миллиграмма (йод, фтор, медь, кобальт и др.).
Железо нормализует состав крови (входя в гемоглобин) и является активным участником окислительных процессов в организме. Оно содержится в печени, почках, яйцах, овсяной и гречневой крупе, ржаном хлебе, яблоках. Суточная потребность в железе – 0,018 г.
Йод участвует в построении и работе щитовидной железы. Вольте всего йода сконцентрировано в морской воде, морской капусте и морской рыбе.
Калий участвует в водном обмене организма человека, усиливая выведение жидкости и улучшая работу сердца.
Он содержится в сухих фруктах (кураге, урюке, черносливе, изюме), горохе, фасоли, картофеле, мясе, рыбе. В сутки человеку необходимо до 5 г калия.
Кальций участвует в построении костей, зубов, необходим для нормальной деятельности нервной системы, сердца, влияет на рост. Солями кальция богаты молочные продукты, яйца, хлеб, овощи, бобовые. Суточная потребность организма в кальции 0,8 г.
Магний влияет на нервную, мышечную и сердечную деятельность, обладает сосудорасширяющим свойством. Содержится во многих овощах, молоке, мясе. Суточная норма потребления магния – 0,4 г.
Медь и кобальт участвуют в кроветворении. Они содержатся в небольших количествах в животной и растительной пище. Медь участвует в тканевом дыхании. Хорошим источником ее являются мясо, рыба, нерыбные морепродукты, гречневая, овсяная и перловая крупы, картофель, абрикосы, груши, крыжовник.
Натрий вместе с калием регулирует водный обмен, задерживая влагу в организме, поддерживает величину осмотического давления в тканях. В пищевых продуктах натрия мало, поэтому его вводя г с поваренной солью (NаСl). Суточная потребность – 4-6 г натрия или 10-15 г поваренной соли.
Сера входит в состав некоторых аминокислот, витамина В1, гормона инсулина. Содержится она в горохе, овсяной крупе, сыре, яйцах, мясе, рыбе. Суточная потребность в сере 1 г.
Фосфор участвует в обмене белков и жиров, в формировании костной ткани, влияет на центральную нервную систему. Содержится в молочных продуктах, яйцах, мясе, рыбе, хлебе, бобовых. Потребность в фосфоре составляет 1,2 г в сутки.
Фтор принимает участие в формировании зубов и костного скелета, содержится в питьевой воде.
Хлор участвует в регуляции осмотического давления в тканях и в образовании соляной кислоты (НС1) в желудке. Поступает хлор с поваренной солью. Суточная потребность в нем – 5-7 г.
Цинк необходим для нормальной функции эндокринной системы. Он обладает липотропными кроветворными свойствами и входит в состав ферментов, обеспечивающих процессы дыхания. Цинком богаты мясо и внутренние органы животных, яйца, рыба, грибы.
Общая суточная потребность организма взрослого человека в минеральных веществах составляет 20 -25 г, при этом важна сбалансированность отдельных элементов. Так, соотношение кальция, фосфора и магния в питании должно составлять 1: 1,5: 0,5, что определяет уровень усвоения этих минеральных веществ в организме.
Для поддержания в организме кислотно-щелочного равновесия необходимо правильно сочетать в питании продукты, содержащие минеральные вещества щелочного действия (Ca, Mg, K, Na), которыми богаты молоко, овощи, фрукты, картофель, и кислотного действия (P, S, Cl), которые содержатся в мясе, рыбе, яйцах, хлебе, крупах.
Интересное о соли неорганической и органической
| Соль – хлористый натрий, используется человеком вместе с пищей, а если быть точным вместо пищи довольно давно. Человек ест соль с кашей, соль с хлебом, соль с супом, соль с салатом, соль с мясом и с другими блюдами. Но удивительно то, что без соли большинство этих блюд перестают быть вкусными, а некоторые даже съедобными – становясь тем, чем они и являются на самом деле. Сложно даже представить, сколько бы продуктов люди навсегда перестали употреблять, если бы их просто лишили соли. Но добавляя соль, человек обманывает свой вкус, и приготовленная им пища как бы становится вкусной. Однако то, что обычная соль весьма негативно сказывается на организме можно судить хотя бы по тому, что смертельная доза соли для человека составляет всего 240 гр. (из расчёта по 3 гр. на 1 кг. веса). Что бы справится с излишками соли организм накапливает воду, по этому съев что то пересоленное хочется пить. Хорошо известна особенность соли задерживать жидкость. Увеличение жидкости помогает организму растворить избытки соли, снижая её концентрацию в тканях, что в результате приводит к увеличению веса. Неорганическая соль способна убивать различные микроорганизмы (не только вредные, но и полезные) – поэтому она широко применяется для консервирования. Известно, что когда соль попадает на рану, или в слизистую оболочку носа, глаз – она начинает разъедать кожу. Можно представить, что происходит в желудке с нашими тканями и микроорганизмами, когда туда попадает мёртвая соль. Как известно, человек на 70-80% состоит из воды. Если в организм ввести неорганическую соль – ускоряется передача нервных импульсов в мозг, нервная система перегревается и изнашивается, что в результате приводит к её старению. Соль заглушая сигналы тревоги, подаваемые организмом, и даёт нам ощущение ложного спокойствия, умиротворения. Многие учёные уверены, что соль необходима организму – и она участвует во многих важных процессах его жизнедеятельности. Да, действительно, но только если речь идёт об органической соли. Всё дело в том, что человеческий организм способен усваивать только органические, то есть живые соединения. А неорганические, или иначе говоря – мёртвые соединения он способен только выводить или откладывать. Поглощение неорганической соли для получения из нее органической так же не возможно для человека, как извлечение органического железа при помощи длительного сосания металлической монеты. Откуда же берётся органическая соль? Она может быть получена только из живых организмов, то есть из овощей, фруктов, орехов, злаков и зелени, но никак не из камней! Во время своего роста, растения впитывают из почвы различные минеральные соли и превращают их в органические соединения. Для этой задачи им служат почвенные бактерии, живущие на поверхности корней. В отличие от мёртвой, неорганической (каменной и морской) соли, эта соль полностью усваивается организмом, не принося ему вреда, в виде различных отложений и избыточного накопления жидкости. При термической обработке органическая соль разрушаются, что подтверждает наличие в ней живых веществ. Живая соль не вызывает привыкания и не парализует работу вкусовых рецепторов во рту, поскольку она не меняет электропроводности в жидкостях человеческого тела. Словом, это безопасное и во всех отношениях полезное вещество, которое мы можем получать из любой живой пищи – как то овощи, фрукты, злаки, орехи или зелень. Таким образом, бывает два вида соли: Мёртвая, неорганическая соль – это каменная и морская, такая соль не усваивается организмом и причиняет ему большой вред. И живая, или органическая соль, которая действительно необходима нашему организму. Но как быть, если овощи и фрукты бедны органическими солями (поскольку не получали достаточного питания, и выращивались не естественными способами – с применения ядохимикатов, удобрений, перепахиванием земли и т.д.)? Тогда на помощь может прийти живая соль, выделенная натуральным способом из зелёных стеблей растения. |
Оригинал записи и комментарии на LiveInternet.ru
Химическая организация клетки. элементный состав клеток. неорганические вещества вода и минеральные соли
- РАЗДЕЛ 1.
- МОЛЕКУЛЯРНЫЙ УРОВЕНЬ ОРГАНИЗАЦИИ ЖИВОГО
- ТЕМА 2.
ХИМИЧЕСКАЯ ОРГАНИЗАЦИЯ КЛЕТКИ. ЭЛЕМЕНТНЫЙ СОСТАВ КЛЕТОК. НЕОРГАНИЧЕСКИЕ ВЕЩЕСТВА: ВОДА И МИНЕРАЛЬНЫЕ СОЛИ
1. Основные вопросы теории
Молекулярный уровень организации живого
Это самый низкий уровень организации живого, представленный отдельными молекулами органических и неорганических веществ, входящих в состав клеток организма. Жизнь можно представить как организационную иерархию вещества.
В живых существах элементы образуют очень сложные органические молекулы, из которых в свою очередь состоят клетки, а из тех – целый организм.
Жизнедеятельность всех живых систем проявляется во взаимодействии молекул различных химических веществ.
Элементный состав клетки
В составе живой природы обнаружено более 80 химических элементов, 27 из них выполняют определенные функции.
| 27 | ||
| ↓ | ↓ | ↓ |
| макроэлементы | микроэлементы | ультрамикроэлементы |
| 99 % | 10-3 % | 10-6 % |
| 98% – биогенные: О, С, Н, NK, Na, Ca, Mg, Fe, Cl, S, P. | B, Mn, Zn, Cu, Co, F, I, Br, Mo. | U, Au, Be, Hg, Se, Ra, Cs. |
Некоторые организмы – интенсивные накопители определенных элементов: бактерии способны накапливать марганец, морские водоросли – йод, ряска – радий, моллюски и ракообразные – медь, позвоночные – железо.
Каждый из химических элементов выполняет важную функцию в клетке.
| Элемент | Биологическая роль |
| О, Н | входят в состав воды. |
| С, О, Н, N | входят в состав белков, липидов, нуклеиновых кислот, полисахаридов. |
| K, Na, Cl | обеспечивают проведение нервного импульса. |
| Ca | компонент костей, зубов, необходим для мышечногосокращения, компонент свертывания крови, посредник в механизме действия гормонов. |
| Mg | структурный компонент хлорофилла, поддерживаетработу рибосом и митохондрий. |
| Fe | структурный компонент гемоглобина, миоглобина. |
| S | входит в состав серосодержащих аминокислот, белков. |
| P | входит в состав нуклеиновых кислот, костной ткани. |
| B | необходим некоторым растениям. |
| Mn, Zn, Cu | активаторы ферментов, влияют на процессы тканевого дыхания. |
| Zn | входит в состав инсулина. |
| Cu | входит в состав окислительных ферментов, переносит кислород в тканях моллюсков. |
| Co | входит в состав витамина В12. |
| F | входит в состав эмали зубов. |
| I | входит в состав тироксина. |
| Химические вещества клетки | |
| ↓ | ↓ |
| неорганические | органические |
| вода – 7585%;минеральные соли – 11,5%. |
|
Уникальное строение воды, её свойства и роль в живой природе
| Строение и свойства воды | Биологические функции воды |
| 1. Малые размеры молекул воды, молекула воды нелинейна. |
Биология. 11 класс
В состав живых организмов входят разнообразные химические соединения, образованные атомами различных элементов. Ключевую роль в осуществлении процессов жизнедеятельности играют органические вещества — белки, углеводы, липиды, нуклеиновые кислоты и др.
, которые в неживой природе практически не встречаются. Однако не все соединения, присущие организмам, специфичны только для живой природы.
Такие неорганические вещества, как вода, неорганические (минеральные) соли и кислоты, широко распространены и в неживой природе.
Вода. В количественном отношении первое место среди веществ, входящих в состав живых организмов, занимает вода. Ее массовая доля в организмах в среднем составляет 65—80 %. Количество воды неодинаково в разных тканях и органах.
Так, в сочных плодах растений может содержаться до 98 % воды, а в зерновках злаков, семенах подсолнечника, льна, бобовых ее массовая доля составляет 7—14 %. Плазма крови, лимфа, тканевая жидкость, секреты большинства желез животных более чем на 90 % состоят из воды.
В скелетных мышцах человека массовая доля воды составляет около 76 %, а в жировой ткани — приблизительно 30 %. С возрастом содержание воды в организме постепенно снижается.
*Организм человека в эмбриональном периоде содержит до 95 % воды. Далее массовая доля воды уменьшается до 80 % (в среднем) у детей, 60—65 % в организме взрослого человека и 45—50 % у пожилых людей. Чем выше содержание воды в клетках и организме в целом, тем интенсивнее протекают процессы обмена веществ.
Человек, потерявший до 50 % массы тела в результате голодания, может остаться в живых, но потеря в результате обезвоживания 20—25 % воды является смертельной. Без употребления воды человек способен прожить не более 3—4 дней.*
Из курса химии вы знаете, что в молекуле воды (Н2О) два атома водорода соединены с атомом кислорода ковалентными полярными связями. Связи Н—О—Н расположены под углом 104,5° друг к другу. Кислород обладает большей электроотрицательностью, чем водород, поэтому атом кислорода притягивает к себе общие электронные пары и приобретает частичный отрицательный заряд. Атомы водорода приобретают частичный положительный заряд, т. е. молекула воды является полярной (рис. 2.1).
Между атомом кислорода одной молекулы воды и атомом водорода другой молекулы возникает электростатическое притяжение. Такое взаимодействие, более слабое, чем ионная связь, называется водородной связью. Каждая молекула воды притягивает к себе за счет образования водородных связей еще четыре молекулы (рис. 2.2).
Таким образом, молекулы воды связаны друг с другом. Поэтому вода при температурах от 0 °С до 100 °С может сохранять жидкое агрегатное состояние, тогда как подобные ей водородные соединения (например, H2S, NH3, HF) являются газами.
Роль воды в живых организмах связана с ее свойствами, прежде всего с малыми размерами молекул, их полярностью и способностью образовывать водородные связи между собой и с другими соединениями.
Благодаря полярности молекулы воды способны формировать так называемые гидратные оболочки вокруг ионов и полярных молекул. Это способствует обособлению частиц и препятствует их склеиванию друг с другом, что особенно важно, например, для белковых молекул.
Полярность молекул и способность образовывать водородные связи делает воду универсальным растворителем для полярных веществ, лучшим, чем большинство жидкостей.
В зависимости от степени взаимодействия с молекулами воды соединения делят на гидрофильные и гидрофобные.
Гидрофильными являются полярные вещества, которые активно взаимодействуют с молекулами воды за счет образования многочисленных водородных связей, что и обусловливает их хорошую растворимость (рис. 2.3, а).
К гидрофильным соединениям относятся низшие спирты и карбоновые кислоты, моносахариды, дисахариды и др. Неполярные вещества являются гидрофобными, они не формируют водородные связи с молекулами воды и не растворяются в ней (рис. 2.3, б). Это высшие карбоновые кислоты, жиры и некоторые другие соединения.
Растворение веществ способствует повышению их реакционной способности, т. к. молекулы или ионы получают возможность более свободно перемещаться и взаимодействовать друг с другом. Большинство химических реакций в живых организмах протекает именно в водных растворах.
Таким образом, в качестве растворителя вода является основной средой протекания процессов обмена веществ — метаболизма. Кроме того, вода служит средством транспорта растворенных в ней веществ.
Эту функцию она выполняет, например, в составе крови, лимфы, тканевой жидкости, мочи и секретов желез животных, в проводящих тканях растений.
Вода является участником многих биохимических процессов, например фотосинтеза. Кислород, выделяющийся в ходе фотосинтеза, образуется при расщеплении молекул воды. Процессы расщепления сложных органических веществ (белков, полисахаридов, липидов и др.) до более простых соединений являются реакциями гидролиза, т. е. протекают при непосредственном участии воды.
Вода практически несжимаема, что важно для поддержания упругости клеток и тканей. Она определяет объем клеток и тургорное давление — давление внутреннего содержимого клетки на ее оболочку. Несжимаемость воды позволяет ей выполнять функцию гидроскелета у круглых и кольчатых червей.
Хорошие смазывающие свойства воды способствуют уменьшению трения в различных частях организма (вспомните роль жидкостей, содержащихся в плевральной полости, околосердечной сумке, полостях суставных сумок человека).
*Каждая молекула жидкости одновременно притягивается ко всем окружающим ее молекулам. При этом силы притяжения, противоположные по направлению, взаимно уравновешивают (компенсируют) друг друга. Поверхностный слой жидкости обладает особыми свойствами, т. к.
его молекулы не имеют «соседей» снаружи и притягиваются только друг к другу и к молекулам, находящимся внутри жидкости. Вследствие этого на поверхности образуется так называемая пленка поверхностного натяжения.
Из всех жидкостей, кроме ртути, вода обладает самым высоким поверхностным натяжением.
Поверхностное натяжение воды определяет форму клеток, их способность захватывать твердые частицы и капли жидкости. Мелкие организмы, например водомерки, личинки комаров, используют пленку поверхностного натяжения воды для передвижения или прикрепления к ней, а некоторые водные и прибрежные растения — для распространения пыльцы и семян.
*Кроме того, поверхностное натяжение воды, а также ее способность взаимодействовать с другими веществами (например, за счет формирования водородных связей) обусловливает свойство капиллярности — способности подниматься или опускаться по узким каналам (капиллярам) и проходить через поры (рис. 2.4). Капиллярность играет важную роль в поднятии растворов по сосудам и трахеидам растений, движении крови, лимфы и других жидкостей по системе мелких сосудов в организме животных.
Вода обладает высокой теплоемкостью. Это значит, что при поглощении или выделении большого количества теплоты температура самой воды изменяется незначительно. Поэтому даже резкие температурные колебания в окружающей среде не приводят к существенному изменению температуры внутри организма.
При переходе жидкой воды в состояние пара происходит разрушение всех водородных связей между ее молекулами, а это требует значительных затрат энергии. Поэтому испарение воды сопровождается охлаждением и используется живыми организмами для защиты от перегрева (потоотделение у млекопитающих, транспирация у растений).
Вода имеет относительно высокую для жидкостей теплопроводность. Движение воды (циркуляция крови у животных, восходящий и нисходящий ток растворов у растений и т. д.) в сочетании с высокой теплопроводностью способствует равномерному распределению теплоты в организме.
Важнейшие биологические функции воды представлены в таблице 2.1.
Таблица 2.1. Основные функции воды в живых организмах
| Функция | Пояснение |
| Структурная | Входит в состав всех клеток, межклеточного вещества, внутренней среды организма, секретов желез и т. д., придает упругость клеткам и тканям, у некоторых животных выполняет функцию гидроскелета |
| Метаболическая | Является средой протекания и участником биохимических реакций |
| Транспортная | Способствует всасыванию растворенных веществ, их перемещению в организме и выведению конечных продуктов обмена веществ |
| Терморегуляторная | Участвует в регуляции теплового режима организмов |
Неорганические вещества клетки. Роль воды и минеральных солей
Вода. Из неорганических веществ, входящих в состав клетки, важнейшим является вода. Количество ее составляет от 60 до 95% общей массы клетки. Вода играет важнейшую роль в жизни клеток и живых организмов в целом. Помимо того что она входит в их состав, для многих организмов это еще и среда обитания.
Вода как компонент биологических систем выполняет следующие важнейшие функции:
Вода—универсальный растворитель для полярных веществ, например солей, Сахаров, спиртов, кислот и др. Вещества, хорошо растворимые в воде, называются гидрофильными.
Когда вещество переходит в раствор, его молекулы или ионы получают возможность двигаться более свободно; соответственно возрастает реакционная способность вещества. Именно по этой причине большая часть химических реакций в клетке протекает в водных растворах.
Ее молекулы участвуют во многих химических реакциях, например при образовании или гидролизе полимеров. В процессе фотосинтеза вода является донором электронов, источником ионов водорода и свободного кислорода.
Неполярные вещества вода не растворяет и не смешивается с ними, поскольку не может образовывать с ними водородные связи. Нерастворимые в воде вещества называются гидрофобными.
Гидрофобные молекулы или их части отталкиваются водой, а в ее присутствии притягиваются друг к другу.
Такие взаимодействия играют важную роль в обеспечении стабильности мембран, а также многих белковых молекул, нуклеиновых кислот и ряда субклеточных структур.
Вода обладает высокой удельной теплоемкостью. Для разрыва водородных связей, удерживающих молекулы воды, требуется поглотить большое количество энергии.
Это свойство обеспечивает поддержание теплового баланса организма при значительных перепадах температуры в окружающей среде.
Кроме того, вода отличается высокой теплопроводностью, что позволяет организму поддерживать одинаковую температуру во всем его объеме.
Вода характеризуется высокой теплотой парообразования, т. е. способностью молекул уносить с собой значительное количество тепла при одновременном охлаждении организма. Благодаря этому свойству воды, проявляющемуся при потоотделении у млекопитающих, тепловой одышке у крокодилов и других животных, транспирации у растений, предотвращается их перегрев.
Для воды характерно исключительно высокое поверхностное натяжение. Это свойство имеет очень важное значение для адсорбционных процессов, для передвижения растворов по тканям (кровообращение, восходящий и нисходящий токи в растениях). Многим мелким организмам поверхностное натяжение позволяет удерживаться на воде или скользить по ее поверхности.
Вода обеспечивает передвижение веществ в клетке и организме, поглощение веществ и выведение продуктов метаболизма.
У растений вода определяет тургор клеток, а у некоторых животных выполняет опорные функции, являясь гидростатическим скелетом (круглые и кольчатые черви, иглокожие).
Вода — составная часть смазывающих жидкостей (синовиальной — в суставах позвоночных, плевральной — в плевральной полости, перикардиальной — в околосердечной сумке) и слизей (облегчают передвижение веществ по кишечнику, создают влажную среду на слизистых оболочках дыхательных путей). Она входит в состав слюны, желчи, слез, спермы и др.
Минеральные соли. Неорганические вещества в клетке, кроме воды, представлены минеральными солями. Молекулы солей в водном растворе распадаются на катионы и анионы. Наибольшее значение имеют катионы (К+, Na+, Са2+, Mg:+, NH4+) и анионы (С1 , Н2Р04 -, НР042- , НС03 -, NO32–, SO4 2- ) Существенным является не только содержание, но и соотношение ионов в клетке.
Разность между количеством катионов и анионов на поверхности и внутри клетки обеспечивает возникновение потенциала действия, что лежит в основе возникновения нервного и мышечного возбуждения. Разностью концентрации ионов по разные стороны мембраны обусловлен активный перенос веществ через мембрану, а также преобразование энергии.
- Анионы фосфорной кислоты создают фосфатную буферную систему, поддерживающую рН внутриклеточной среды организма на уровне 6,9.
- Угольная кислота и ее анионы формируют бикарбонатную буферную систему, поддерживающую рН внеклеточной среды (плазма крови) на уровне 7,4.
- Некоторые ионы участвуют в активации ферментов, создании осмотического давления в клетке, в процессах мышечного сокращения, свертывании крови и др.
Ряд катионов и анионов необходим дпясинтеза важных органических веществ (например, фосфолипидов, АТФ, нуклеоти-дов, гемоглобина, гемоцианина, хлорофилла и др.), а также аминокислот, являясь источниками атомов азота и серы.

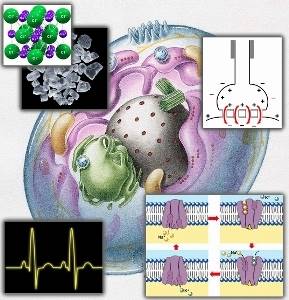 Минеральные соли могут содержаться в организме в растворенном виде (диссоциированными на ионы) или в нерастворимом виде.
Минеральные соли могут содержаться в организме в растворенном виде (диссоциированными на ионы) или в нерастворимом виде.