Обмен веществ — важнейшее свойство живых организмов. Совокупность реакций обмена веществ, протекающих в организме, называется метаболизмом. Метаболизм состоит из реакций ассимиляции (пластического обмена, анаболизма) и реакций диссимиляции (энергетического обмена, катаболизма).
Ассимиляция — совокупность реакций биосинтеза, протекающих в клетке, диссимиляция — совокупность реакций распада и окисления высокомолекулярных веществ, идущих с выделением энергии.
Эти группы реакций взаимосвязаны: реакции биосинтеза невозможны без энергии, которая выделяется в реакциях энергетического обмена, реакции диссимиляции не идут без ферментов, образующихся в реакциях пластического обмена.
По типу обмена веществ организмы подразделяются на две группы: автотрофы и гетеротрофы.
Автотрофы — организмы, способные синтезировать органические вещества из неорганических и использующие для этого синтеза или солнечную энергию, или энергию, выделяющуюся при окислении неорганических веществ.
Гетеротрофы — организмы, использующие для своей жизнедеятельности органические вещества, синтезированные другими организмами. В качестве источника углерода автотрофы используют неорганические вещества (СО2), а гетеротрофы — экзогенные органические.
Источники энергии: у автотрофов — энергия солнечного света (фотоавтотрофы) или энергия, выделяющаяся при окислении неорганических соединений (хемоавтотрофы), у гетеротрофов — энергия окисления органических веществ (хемогетеротрофы).
Большинство живых организмов относится или к фотоавтотрофам (растения), или к хемогетеротрофам (грибы, животные). Если организмы, в зависимости от условий, ведут себя как авто- либо как гетеротрофы, то их называют миксотрофами (эвглена зеленая).
Биосинтез белков
Биосинтез белков является важнейшим процессом анаболизма. Все признаки, свойства и функции клеток и организмов определяются в конечном итоге белками. Белки недолговечны, время их существования ограничено. В каждой клетке постоянно синтезируются тысячи различных белковых молекул. В начале 50-х гг. ХХ в. Ф.
Крик сформулировал центральную догму молекулярной биологии: ДНК → РНК → белок. Согласно этой догме способность клетки синтезировать определенные белки закреплена наследственно, информация о последовательности аминокислот в белковой молекуле закодирована в виде последовательности нуклеотидов ДНК.
Участок ДНК, несущий информацию о первичной структуре конкретного белка, называется геном. Гены не только хранят информацию о последовательности аминокислот в полипептидной цепочке, но и кодируют некоторые виды РНК: рРНК, входящие в состав рибосом, и тРНК, отвечающие за транспорт аминокислот.
В процессе биосинтеза белка выделяют два основных этапа: транскрипция — синтез РНК на матрице ДНК (гена) — и трансляция — синтез полипептидной цепи.
Генетический код и его свойства
Генетический код — система записи информации о последовательности аминокислот в полипептиде последовательностью нуклеотидов ДНК или РНК. В настоящее время эта система записи считается расшифрованной.
Свойства генетического кода:
- триплетность: каждая аминокислота кодируется сочетанием из трех нуклеотидов (триплетом, кодоном);
- однозначность (специфичность): триплет соответствует только одной аминокислоте;
- вырожденность (избыточность): аминокислоты могут кодироваться несколькими (до шести) кодонами;
- универсальность: система кодирования аминокислот одинакова у всех организмов Земли;
- неперекрываемость: последовательность нуклеотидов имеет рамку считывания по 3 нуклеотида, один и тот же нуклеотид не может быть в составе двух триплетов;
- из 64 кодовых триплетов 61 — кодирующие, кодируют аминокислоты, а 3 — бессмысленные (в РНК — УАА, УГА, УАГ), не кодируют аминокислоты. Они называются кодонами-терминаторами, поскольку блокируют синтез полипептида во время трансляции. Кроме того, есть кодон-инициатор (в РНК — АУГ), с которого трансляция начинается.
Таблица генетического кода
* Первый нуклеотид в триплете — один из четырех левого вертикального ряда, второй — один из верхнего горизонтального ряда, третий — из правого вертикального.
Реакции матричного синтеза
Это особая категория химических реакций, происходящих в клетках живых организмов.
Во время этих реакций происходит синтез полимерных молекул по плану, заложенному в структуре других полимерных молекул-матриц.
На одной матрице может быть синтезировано неограниченное количество молекул-копий. К этой категории реакций относятся репликация, транскрипция, трансляция и обратная транскрипция.
Строение гена эукариот
Ген — участок молекулы ДНК, кодирующий первичную последовательность аминокислот в полипептиде или последовательность нуклеотидов в молекулах транспортных и рибосомных РНК. ДНК одной хромосомы может содержать несколько тысяч генов, которые располагаются в линейном порядке. Место гена в определенном участке хромосомы называется локусом.
Особенностями строения гена эукариот являются: 1) наличие достаточно большого количества регуляторных блоков, 2) мозаичность (чередование кодирующих участков с некодирующими). Экзоны (Э) — участки гена, несущие информацию о строении полипептида. Интроны (И) — участки гена, не несущие информацию о строении полипептида.
Число экзонов и интронов различных генов разное; экзоны чередуются с интронами, общая длина последних может превышать длину экзонов в два и более раз. Перед первым экзоном и после последнего экзона находятся нуклеотидные последовательности, называемые соответственно лидерной (ЛП) и трейлерной последовательностью (ТП).
Лидерная и трейлерная последовательности, экзоны и интроны образуют единицу транскрипции. Промотор (П) — участок гена, к которому присоединяется фермент РНК-полимераза, представляет собой особое сочетание нуклеотидов.
Перед единицей транскрипции, после нее, иногда в интронах находятся регуляторные элементы (РЭ), к которым относятся энхансеры и сайленсеры. Энхансеры ускоряют транскрипцию, сайленсеры тормозят ее.
Транскрипция у эукариот
Транскрипция — синтез РНК на матрице ДНК. Осуществляется ферментом РНК-полимеразой.
РНК-полимераза может присоединиться только к промотору, который находится на 3'-конце матричной цепи ДНК, и двигаться только от 3'- к 5'-концу этой матричной цепи ДНК.
Синтез РНК происходит на одной из двух цепочек ДНК в соответствии с принципами комплементарности и антипараллельности.
Строительным материалом и источником энергии для транскрипции являются рибонуклеозидтрифосфаты (АТФ, УТФ, ГТФ, ЦТФ).
В результате транскрипции образуется «незрелая» иРНК (про-иРНК), которая проходит стадию созревания или процессинга.
Процессинг включает в себя: 1) КЭПирование 5'-конца, 2) полиаденилирование 3'-конца (присоединение нескольких десятков адениловых нуклеотидов), 3) сплайсинг (вырезание интронов и сшивание экзонов).
В зрелой иРНК выделяют КЭП, транслируемую область (сшитые в одно целое экзоны), нетранслируемые области (НТО) и полиадениловый «хвост».
Транслируемая область начинается кодоном-инициатором, заканчивается кодонами-терминаторами. НТО содержат информацию, определяющую поведение РНК в клетке: срок «жизни», активность, локализацию.
Транскрипция и процессинг происходят в клеточном ядре. Зрелая иРНК приобретает определенную пространственную конформацию, окружается белками и в таком виде через ядерные поры транспортируется к рибосомам; иРНК эукариот, как правило, моноцистронны (кодируют только одну полипептидную цепь).
Трансляция
Трансляция — синтез полипептидной цепи на матрице иРНК.
Органоиды, обеспечивающие трансляцию, — рибосомы. У эукариот рибосомы находятся в некоторых органоидах — митохондриях и пластидах (70S-рибосомы), в свободном виде в цитоплазме (80S-рибосомы) и на мембранах эндоплазматической сети (80S-рибосомы).
Таким образом, синтез белковых молекул может происходить в цитоплазме, на шероховатой эндоплазматической сети, в митохондриях и пластидах. В цитоплазме синтезируются белки для собственных нужд клетки; белки, синтезируемые на ЭПС, транспортируются по ее каналам в комплекс Гольджи и выводятся из клетки. В рибосоме выделяют малую и большую субъединицы.
Малая субъединица рибосомы отвечает за генетические, декодирующие функции; большая — за биохимические, ферментативные.
В малой субъединице рибосомы расположен функциональный центр (ФЦР) с двумя участками — пептидильным (Р-участок) и аминоацильным (А-участок). В ФЦР может находиться шесть нуклеотидов иРНК, три — в пептидильном и три — в аминоацильном участках.
Для транспорта аминокислот к рибосомам используются транспортные РНК, тРНК (лекция №4). Длина тРНК от 75 до 95 нуклеотидных остатков. Они имеют третичную структуру, по форме напоминающую лист клевера. В тРНК различают антикодоновую петлю и акцепторный участок.
В антикодоновой петле РНК имеется антикодон, комплементарный кодовому триплету определенной аминокислоты, а акцепторный участок на 3'-конце способен с помощью фермента аминоацил-тРНК-синтетазы присоединять именно эту аминокислоту (с затратой АТФ).
Таким образом, у каждой аминокислоты есть свои тРНК и свои ферменты, присоединяющие аминокислоту к тРНК.
Двадцать видов аминокислот кодируются 61 кодоном, теоретически может быть 61 вид тРНК с соответствующими антикодонами.
Но кодируемых аминокислот всего 20 видов, значит, у одной аминокислоты может быть несколько тРНК.
Установлено существование нескольких тРНК, способных связываться с одним и тем же кодоном (последний нуклеотид в антикодоне тРНК не всегда важен), поэтому в клетке обнаружено всего около 40 различных тРНК.
Синтез белка начинается с того момента, когда к 5'-концу иРНК присоединяется малая субъединица рибосомы, в Р-участок которой заходит метиониновая тРНК (транспортирующая аминокислоту метионин).
Следует отметить, что любая полипептидная цепь на N-конце сначала имеет метионин, который в дальнейшем чаще всего отщепляется.
Синтез полипептида идет от N-конца к С-концу, то есть пептидная связь образуется между карбоксильной группой первой и аминогруппой второй аминокислот.
Затем происходит присоединение большой субъединицы рибосомы, и в А-участок поступает вторая тРНК, чей антикодон комплементарно спаривается с кодоном иРНК, находящимся в А-участке.
Пептидилтрансферазный центр большой субъединицы катализирует образование пептидной связи между метионином и второй аминокислотой. Отдельного фермента, катализирующего образование пептидных связей, не существует. Энергия для образования пептидной связи поставляется за счет гидролиза ГТФ.
Как только образовалась пептидная связь, метиониновая тРНК отсоединяется от метионина, а рибосома передвигается на следующий кодовый триплет иРНК, который оказывается в А-участке рибосомы, а метиониновая тРНК выталкивается в цитоплазму. На один цикл расходуется 2 молекулы ГТФ. В А-участок заходит третья тРНК, и образуется пептидная связь между второй и третьей аминокислотами.
Трансляция идет до тех пор, пока в А-участок не попадает кодон-терминатор (УАА, УАГ или УГА), с которым связывается особый белковый фактор освобождения. Полипептидная цепь отделяется от тРНК и покидает рибосому. Происходит диссоциация, разъединение субъединиц рибосомы.
Скорость передвижения рибосомы по иРНК — 5–6 триплетов в секунду, на синтез белковой молекулы, состоящей из сотен аминокислотных остатков, клетке требуется несколько минут. Первым белком, синтезированным искусственно, был инсулин, состоящий из 51 аминокислотного остатка. Потребовалось провести 5000 операций, в работе в течение трех лет принимали участие 10 человек.
В трансляции можно выделить три стадии: а) инициации (образование иницаторного комплекса), б) элонгации (непосредственно «конвейер», соединение аминокислот друг с другом), в) терминации (образование терминирующего комплекса).
Транскрипция и трансляция у прокариот
«Механизмы» сборки полинуклеотидных и полипептидных цепочек у прокариот и эукариот не различаются. Но в связи с тем, что гены прокариот не имеют экзонов и интронов (исключение — гены архебактерий), располагаются группами, и на эту группу генов приходится один промотор, появляются следующие особенности транскрипции и трансляции у прокариот.
- В результате транскрипции образуется полицистронная иРНК, кодирующая несколько белков, совместно обеспечивающих определенную группу реакций.
- иРНК имеет несколько центров инициации трансляции, терминации трансляции и НТО.
- Не происходят КЭПирование, полиаденилирование и сплайсинг иРНК.
- Трансляция начинается еще до завершения транскрипции; эти процессы не разделены во времени и пространстве, как это имеет место у эукариот.
1 — ДНК; 2 — РНК-полимераза; 3 — Нуклеозидтрифосфаты ГТФ, ЦТФ, АТФ, УТФ.
Можно добавить, что срок «жизни» прокариотических иРНК — несколько минут (у эукариот — часы и даже сутки).
- Перейти к лекции №9 « Строение прокариотической клетки. Вирусы»
- Перейти к лекции №11 « Понятие об обмене веществ. Биосинтез белков»
- Смотреть оглавление (лекции №1-25)
Модификация аминокислотных остатков в синтезированном белке называется. Α о бщее строение протеиногенной аминокислоты Аминокислоты
Большая группа реакций постсинтетической модификации белка связана не с разрывом полипептидной цепи (процессинг), а с преобразованием аминокислотных радикалов К. Обычно оно протекает по мере продвижения белковой молекулы по трубочкам и цистернам ЭР и в аппарате Гольджи. Именно в мембранах этих структур локализованы ферменты, распознающие нужные локусы в молекуле белка и катализирующие соответствующее преобразование строго определенных аминокислот.
Общая характеристика
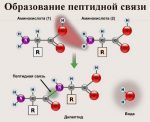
Пептиды — это продукты конденсации двух или более молекул аминокислот. Две молекулы аминокислоты могут реагировать друг с другом с отщеплением молекулы воды и образованием продукта, в котором фрагменты связаны пептидной связью -CO-NH-.
Полученное соединение называют дипептидом. Молекула дипептида, подобно аминокислотам, содержит аминогруппу и карбоксильную группу и может реагировать еще с одной молекулой аминокислоты:
Продукт реакции называется трипептидом. Процесс наращивания пептидной цепи может продолжаться, в принципе, неограниченно и приводить к веществам с очень высокой молекулярной массой (белкам).
Число пептидов, которые могут быть построены из 20 природных аминокислот, огромно. Теоретически можно получить 20n пептидов, содержащих и остатков. Таким образом, может существовать 400 дипептидов, 8000 трипептидов и т.д. При n = 62 число возможных пептидов превосходит число атомов во Вселенной (1080).
Формулы пептидов обычно записывают так, что свободная аминогруппа находится слева (на N-конце цепи), а свободная карбоксильная группа — справа (на С-конце). Основная часть пептидной цепи построена из повторяющихся участков -СН-CO-NH- и боковых групп R, R’ и т.д.
Структуру пептидов, содержащих большое число остатков аминокислот, записывают в сокращенном виде с использованием обозначений, приведенных выше (см. «Аминокислоты», «Общая характеристика»). Например, строение молекулы вазопрессина — пептида, построенного из 9 аминокислотных остатков, можно изобразить следующим образом:
- Структурная формула вазопрессина.
- Эту же структуру можно изобразить в сокращенном виде с использованием трехбуквенных и однобуквенных обозначений аминокислот:
- Сокращенное представление молекулы вазопрессина.
Обратите внимание на то, что в этом пептиде остатки цистеина связаны дисульфидным мостиком. С-конец цепи содержит амидную группу -СО-NН2 вместо карбоксильной.
Химические свойства
Основное свойство пептидов — способность к гидролизу.
При гидролизе происходит полное или частичное расщепление пептидной цепи и образуются более короткие пептиды с меньшей молекулярной массой или α-аминокислоты, составляющие цепь.
Анализ продуктов полного гидролиза позволяет установить аминокислотный состав пептида. Полный гидролиз происходит при длительном нагревании пептида с концентрированной соляной кислотой.
Последовательность аминокислот в цепи может быть установлена путем частичного гидролиза пептида. Для этого необходимо последовательно, одну за другой, отщеплять аминокислоты от одного из концов цепи и устанавливать их структуру.
Гидролиз пептидов может происходить в кислой или щелочной среде, а также под действием ферментов. В кислой и щелочной средах образуются соли аминокислот. Ферментативный гидролиз важен тем, что протекает селективно, т.е.
позволяет расщеплять строго определенные участки пептидной цепи. Интересно, что селективный гидролиз может протекать и под действием неорганических реагентов.
Так, бромистый циан (BrCN) расщепляет полипептидную цепь только по пептидной связи, образованной карбоксильной группой метионина
Биологическое значение. Многие пептиды проявляют биологическую активность. Простейший из них — трипептид глутатион, который относится к классу гормонов — веществ, регулирующих процессы жизнедеятельности.
Этот гормон построен из остатков аланина, цистеина и глутаминовой кислоты. Известны гормоны, содержащие 9 аминокислотных остатков, — вазопрессин и окситоцин.
Вазопрессин повышает кровяное давление, а окситоцин стимулирует выделение молока молочными железами.
Пептидная связь: образование, строение … Пептидная связь Аминокислоты. Пептиды. Белки …
Своё Спасибо, еще не выражали..
Пептидная связь
- Образование пептидной связи между двумя аминокислотами происходит следующим образом:
- Именно из-за амфотерности растворы аминокислот имеют буферные свойства, то есть они способны поддерживать постоянный уровень pH.
- Пептидной называют ковалентную связь, возникающую между аминогруппой одной аминокислоты и карбоксильной группой другой аминокислоты.
Соединения, которые при этом образуются, называют пептидами.
В зависимости от количества остатков аминокислот, участвующих в реакции поликонденсации, образованные соединения называют ди-, три-, тетра- или полипептидами. Пептид имеет две свободные функциональные группы – аминогруппу и карбоксильную группу.
Способность образовывать пептидные связи имеет фундаментальное значение для живых организмов, ведь именно благодаря этому аминокислоты соединяются друг с другом, образуя пептиды и белки.
Свойства пептидной связи [ | ]
- Как и в случае любых амидов, в пептидной связи за счет резонанса канонических структур связь C-N между углеродом карбонильной группы и атомом азота частично имеет характер двойной:
- Это проявляется, в частности, в уменьшении её длины до 1,33 ангстрема:
- Это обусловливает следующие свойства:
- 4 атома связи (C, N, O и H) и 2 α-углерода находятся в одной плоскости. R-группы аминокислот и водороды при α-углеродах находятся вне этой плоскости.
- H и O в пептидной связи, а также α-углероды двух аминокислот транс-ориентированы (транс-изомер более устойчив). В случае L-аминокислот, что имеет место во всех природных белках и пептидах, R-группы также транс-ориентированы.
- Вращение вокруг связи C-N затруднено, возможно вращение вокруг С-С связи.
Для обнаружения белков и пептидов, а также их количественного определения в растворе используют биуретовую реакцию.
Свойства пептидной связи
- Как и в случае любых амидов, в пептидной связи за счет резонанса канонических структур связь C-N между углеродом карбонильной группы и атомом азота частично имеет характер двойной:
- Это проявляется, в частности, в уменьшении её длины до 1,33 ангстрема:
- Это обусловливает следующие свойства:
- 4 атома связи (C, N, O и H) и 2 α-углерода находятся в одной плоскости. R-группы аминокислот и водороды при α-углеродах находятся вне этой плоскости.
- H и O в пептидной связи, а также α-углероды двух аминокислот трансориентированы (транс-изомер более устойчив). В случае L-аминокислот, что имеет место во всех природных белках и пептидах, R-группы также трансориентированы.
- Вращение вокруг связи C-N затруднено, возможно вращение вокруг С-С связи.
Для обнаружения белков и пептидов, а также их количественного определения в растворе используют биуретовую реакцию.
Первичная структура — последовательность аминокислот в полипептидной цепи. Важными особенностями первичной структуры являются консервативные мотивы — сочетания аминокислот, играющих ключевую роль в функциях белка. Консервативные мотивы сохраняются в процессе эволюции видов, по ним часто удаётся предсказать функцию неизвестного белка.
Структуры
Пептидная связь
В белках аминокислотные остатки связаны между собой с помощью пептидных связей (разновидность ковалентных амидных связей) ( 3 ), в образовании которых участвуют карбоксильная группа одной аминокислоты и аминогруппа другой ( 4 ▼ ).
Радикалы аминокислот, как правило, не принимают участие в образовании пептидных связей, однако есть и исключения. Пример: пептидглутатион имеет пептидную связь между аминогруппой цистеина и карбоксильной группой боковой цепи глутамата.
Пептидная группасвязи C-N
Рис. 3. Пептидная связь.
Рис. 4. Образование пептидной связи между двумя аминокислотами.
Рис. 5. Пептидная группа. Длина химических связей выражена в ангстремах (Å), а углы — в градусах.
Длина пептидной связи C-N на 0,13 Å1 короче длины простой ковалентной связи C-N. Иными словами, пептидная связь имеет характер «полудвойной» ковалентной связи.
- Конформация и торсионные углы полипептидного скелета стерически фиксированы, поскольку вращение вокруг связей Cα -C2 и Cα -N привело бы к чрезмерному сближению атомов амидноговодорода , карбонильногокислорода или радикала ( 6 ▼ ).
- 1 Ангстрем — единица измерения расстояний. 1 Å = 1,0 × 10–10 м = 0,1 нм
- 2 C α — α-атом углерода в молекуле аминокислоты (атом, с которым связана амино- и карбоксильная группа).
Рис. 6. Торсионные углы полипептидного ске-
лета. На рисунке показаны две плоские пептидные группы. Вращение возможно только относительно связей Cα -C (ψ) и Cα -N (φ). Углы этого вращения обозначены как φ и ψ.
Синтез белков обеспечивают рибосомы
Трансляция (англ. translation – перевод) – это биосинтез белка на матрице мРНК.
После переноса информации с ДНК на матричную РНК начинается синтез белков. Каждая зрелая мРНК несет информацию только об одной полипептидной цепи. Если клетке необходимы другие белки, то необходимо транскрибировать мРНК с иных участков ДНК.
Биосинтез белков или трансляция происходит на рибосомах, внутриклеточных белоксинтезирующих органеллах, и включает 5 ключевых элементов:
- матрица – матричная РНК,
- растущая цепь – полипептид,
- субстрат для синтеза – 20 протеиногенных аминокислот,
- источник энергии – ГТФ,
- рибосомальные белки, рРНК и белковые факторы.
Выделяют три основных стадии трансляции: инициация, элонгация, терминация.
Инициация
Для инициации необходимы мРНК, ГТФ, малая и большая субъединицы рибосомы, три белковых фактора инициации (ИФ-1, ИФ-2, ИФ-3), метионин и тРНК для метионина.
В начале этой стадии формируются два тройных комплекса:
- первый комплекс – мРНК + малая субъединица + ИФ-3,
- второй комплекс – метионил-тРНК + ИФ-2 + ГТФ.
После формирования тройные комплексы объединяются с большой субъединицей рибосомы. В этом процессе активно участвуют белковые факторы инициации, источником энергии служит ГТФ.
После сборки комплекса инициирующая метионил-тРНК связывается с первым кодоном АУГ матричной РНК и располагается в П-центре (пептидильный центр) большой субъединицы.
А-центр (аминоацильный центр) остается свободным, он будет задействован на стадии элонгации для связывания аминоацил-тРНК.
События стадии инициации
После присоединения большой субъединицы начинается стадия элонгации.
Элонгация
Для этой стадии необходимы все 20 аминокислот, тРНК для всех аминокислот, белковые факторы элонгации, ГТФ. Удлинение цепи происходит со скоростью примерно 20 аминокислот в секунду.
Элонгация представляет собой циклический процесс. Первый цикл (и следующие циклы) элонгации включает три шага:
- Присоединение аминоацил-тРНК (еще второй) к кодону мРНК (еще второму), аминокислота при этом встраивается в А-центр рибосомы. Источником энергии служит ГТФ.
- Фермент пептидилтрансфераза осуществляет перенос метионина с метионил-тРНК (в П-центре) на вторую аминоацил-тРНК (в А-центре) с образованием пептидной связи между метионином и второй аминокислотой. При этом уже активированная СООН-группа метионина связывается со свободной NH2-группой второй аминокислоты. Здесь источником энергии служит макроэргическая связь между аминокислотой и тРНК.
- Фермент транслоказа перемещает мРНК относительно рибосомы таким образом, что первый кодон АУГ оказывается вне рибосомы, второй кодон (на рисунке ) становится напротив П-центра, напротив А-центра оказывается третий кодон (на рисунке ). Для этих процессов необходима затрата энергии ГТФ. Так как вместе с мРНК перемещаются закрепленные на ней тРНК, то инициирующая первая тРНК выходит из рибосомы, вторая тРНК с дипептидом помещается в П-центр.
Последовательность событий стадии элонгации
Второе повторение цикла – начинается с присоединения третьей аминоацил-тРНК к третьему кодону мРНК, аминокислота-3 становится в А-центр. Далее трансферазная реакции повторяется и образуется трипептид, занимающий А-центр, после чего он смещается в П-центр в транслоказной реакции..
В пустой А-центр входит четвертая аминоацил-тРНК и начинается третий цикл элонгации:
Образование пептидной связи при встраивании четвертой аминокислоты в пептид. Субъединицы рибосомы, большая часть транспортных РНК и матричная РНК не показаны
Цикл элонгации (реакции 1,2,3) повторяется столько раз, сколько аминокислот необходимо включить в полипептидную цепь.
Терминация
Синтез белка продолжается до тех пор, пока рибосома не достигнет на мРНК особых терминирующих кодонов – стоп-кодонов УАА, УАГ, УГА. Данные триплеты не кодируют ни одной из аминокислот, их также называют нонсенс-кодоны. При вхождении этих кодонов внутрь рибосомы происходит активация белковых факторов терминации, которые последовательно катализируют:
- Гидролитическое отщепление полипептида от конечной тРНК.
- Отделение от П-центра последней, уже пустой, тРНК.
- Диссоциацию рибосомы.
Источником энергии для завершения трансляции является ГТФ.
Реакции стадии терминации
Полирибосомы
По причине того, что продолжительность жизни матричной РНК невелика, перед клеткой стоит задача использовать ее максимально эффективно, т.е. получить максимальное количество “белковых копий”.
- Для достижения этой цели на каждой мРНК может располагаться не одна, а несколько рибосом, встающих последовательно друг за другом и синтезирующих пептидные цепи.
- Такие образования называются полирибосомы.
- Вы можете спросить или оставить свое мнение.
- Download SocComments v1.3
Синтез белков обеспечивают рибосомы
Трансляция (англ. translation – перевод) – это биосинтез белка на матрице мРНК.
После переноса информации с ДНК на матричную РНК начинается синтез белков. Каждая зрелая мРНК несет информацию только об одной полипептидной цепи. Если клетке необходимы другие белки, то необходимо транскрибировать мРНК с иных участков ДНК.
Биосинтез белков или трансляция происходит на рибосомах, внутриклеточных белоксинтезирующих органеллах, и включает 5 ключевых элементов:
- матрица – матричная РНК,
- растущая цепь – полипептид,
- субстрат для синтеза – 20 протеиногенных аминокислот,
- источник энергии – ГТФ,
- рибосомальные белки, рРНК и белковые факторы.
Выделяют три основных стадии трансляции: инициация, элонгация, терминация.
Инициация
Для инициации необходимы мРНК, ГТФ, малая и большая субъединицы рибосомы, три белковых фактора инициации (ИФ-1, ИФ-2, ИФ-3), метионин и тРНК для метионина.
В начале этой стадии формируются два тройных комплекса:
- первый комплекс – мРНК + малая субъединица + ИФ-3,
- второй комплекс – метионил-тРНК + ИФ-2 + ГТФ.
После формирования тройные комплексы объединяются с большой субъединицей рибосомы. В этом процессе активно участвуют белковые факторы инициации, источником энергии служит ГТФ.
После сборки комплекса инициирующая метионил-тРНК связывается с первым кодоном АУГ матричной РНК и располагается в П-центре (пептидильный центр) большой субъединицы.
А-центр (аминоацильный центр) остается свободным, он будет задействован на стадии элонгации для связывания аминоацил-тРНК.
События стадии инициации
После присоединения большой субъединицы начинается стадия элонгации.
Элонгация
Для этой стадии необходимы все 20 аминокислот, тРНК для всех аминокислот, белковые факторы элонгации, ГТФ. Удлинение цепи происходит со скоростью примерно 20 аминокислот в секунду.
Элонгация представляет собой циклический процесс. Первый цикл (и следующие циклы) элонгации включает три шага:
- Присоединение аминоацил-тРНК (еще второй) к кодону мРНК (еще второму), аминокислота при этом встраивается в А-центр рибосомы. Источником энергии служит ГТФ.
- Фермент пептидилтрансфераза осуществляет перенос метионина с метионил-тРНК (в П-центре) на вторую аминоацил-тРНК (в А-центре) с образованием пептидной связи между метионином и второй аминокислотой. При этом уже активированная СООН-группа метионина связывается со свободной NH2-группой второй аминокислоты. Здесь источником энергии служит макроэргическая связь между аминокислотой и тРНК.
- Фермент транслоказа перемещает мРНК относительно рибосомы таким образом, что первый кодон АУГ оказывается вне рибосомы, второй кодон (на рисунке ) становится напротив П-центра, напротив А-центра оказывается третий кодон (на рисунке ). Для этих процессов необходима затрата энергии ГТФ. Так как вместе с мРНК перемещаются закрепленные на ней тРНК, то инициирующая первая тРНК выходит из рибосомы, вторая тРНК с дипептидом помещается в П-центр.
Последовательность событий стадии элонгации
Второе повторение цикла – начинается с присоединения третьей аминоацил-тРНК к третьему кодону мРНК, аминокислота-3 становится в А-центр. Далее трансферазная реакции повторяется и образуется трипептид, занимающий А-центр, после чего он смещается в П-центр в транслоказной реакции..
В пустой А-центр входит четвертая аминоацил-тРНК и начинается третий цикл элонгации:
Образование пептидной связи при встраивании четвертой аминокислоты в пептид.Субъединицы рибосомы, большая часть транспортных РНК и матричная РНК не показаны
Цикл элонгации (реакции 1,2,3) повторяется столько раз, сколько аминокислот необходимо включить в полипептидную цепь.
Терминация
Синтез белка продолжается до тех пор, пока рибосома не достигнет на мРНК особых терминирующих кодонов – стоп-кодонов УАА, УАГ, УГА. Данные триплеты не кодируют ни одной из аминокислот, их также называют нонсенс-кодоны. При вхождении этих кодонов внутрь рибосомы происходит активация белковых факторов терминации, которые последовательно катализируют:
- Гидролитическое отщепление полипептида от конечной тРНК.
- Отделение от П-центра последней, уже пустой, тРНК.
- Диссоциацию рибосомы.
Источником энергии для завершения трансляции является ГТФ.
Реакции стадии терминации
Полирибосомы
По причине того, что продолжительность жизни матричной РНК невелика, перед клеткой стоит задача использовать ее максимально эффективно, т.е. получить максимальное количество “белковых копий”.
Для достижения этой цели на каждой мРНК может располагаться не одна, а несколько рибосом, встающих последовательно друг за другом и синтезирующих пептидные цепи.
Такие образования называются полирибосомы.
Трансляция
☰
Под трансляцией в биологии понимают синтез из аминокислот полипептидов, который протекает в цитоплазме на рибосомах при участии 1) мРНК в качестве матрицы, 2) тРНК в качестве переносчика аминокислот, а также 3) ряда белковых факторов, выполняющих каталитическую функцию на разных этапах процесса. Трансляция протекает в клетках всех живых организмов, это фундаментальный процесс живой природы.
С информационной точки зрения трансляцию можно определить как механизм перевода последовательности триплетов мРНК в последовательность аминокислот белка.
Функция рибосом состоит в удерживании в нужном положении мРНК, тРНК и белковых факторов до тех пор, пока не произойдет определенная химическая реакция. Чаще всего это образование пептидной связи между соседними аминокислотами.
Трансляция и биосинтез белка обычно означают одно и то же. Однако, когда говорят о биосинтезе белка, то нередко в него включают посттрансляционные модификации полипептидов (приобретение ими вторичной, третичной и четверичной структур), а также иногда могут включать процесс транскрипции. С этой точки зрения трансляция рассматривается как важный этап в биосинтезе белков.
Процесс трансляции у эукариот и прокариот имеет ряд отличий, в основном связанный с разнообразием и активностью белковых факторов.
На одной цепочке мРНК может находится несколько рибосом, образуя полисому. При этом сразу происходит синтез нескольких идентичных полипептидов (но каждый находится на своей стадии синтеза).
Синтез одного белка обычно длится несколько секунд.
Аминокислоты, из которых синтезируется полипептид, обязательно проходят стадию активации. Сам же процесс трансляции включает три стадии: инициацию, элонгацию и терминацию.
Процесс трансляции обладает свойством специфичности. Во-первых, определенным кодонам мРНК соответствуют свои тРНК. Во вторых, аминокислоты присоединяются только к «своим» тРНК.
Активация аминокислот
Активация аминокислот необходима, так как только в таком состоянии они способны соединяться с тРНК и позже образовывать между собой пептидные связи.
В цитоплазме клеток всегда находятся свободные (не соединенные с другими веществами) аминокислоты. Специфичные ферменты в присутствии АТФ преобразуют аминокислоту в аминоациладенилат, который уже способен соединяться с тРНК.
Существует класс ферментов – аминоацил-тРНК-синтетазы, – которые активируют аминокислоты, используя при этом энергию АТФ. Каждая аминокислота активируется своим ферментом, после чего присоединяется только к своей тРНК. Образуется комплекс аминокислоты с тРНК – аминоацил-тРНК (аа-тРНК).
Инициация трансляции включает следующие последовательно протекающие при участии факторов инициации этапы:
-
Присоединение 5'-конца мРНК к малой субъединице рибосомы. При этом стартовый кодон (AUG) размещается в недостроенном (из-за отсутствия большой субъединицы) P-сайте рибосомы.
-
Комплекс аа-тРНК с соответствующим антикодоном присоединяется к стартовому кодону мРНК. У эукариот кодон AUG кодирует аминокислоту метионин, у прокариот — формил-метионин. Позже эти стартовые аминокислоты вырезаются из готового полипептида.
-
Происходит объединение субъединиц рибосом, в результате чего достраиваются их P- и A-сайты.
Схема строения рибосомы (A, P, E — участки-сайты для молекул тРНК)
Таким образом, на этапе инициации происходит распознавание рибосомой стартового кодона и подготовка к началу синтеза.
Образующаяся связь между рибосомой и мРНК обратима, мРНК после синтеза полипептида может быть отсоединена от рибосомы. В последствии мРНК используется еще раз или разрушается специальными ферментами.
Стартовый кодон AUG отличается от других таких же кодонов в середине мРНК тем, что перед ним находится кэп и определенные нуклеотидные последовательности. Именно благодаря им AUG распознается как стартовый. (Это касается в основном эукариот.)
Элонгация трансляции
На этом этапе происходит непосредственный синтез полипептидной цепочки. Процесс элонгации состоит из множества циклов. Один цикл элонгации — это присоединение одной аминокислоты к растущей полипептидной цепочке.
Уже на этапе инициации P-сайт рибосомы оказывается занятым первой тРНК, несущей аминокислоту метионин. В первом цикле элонгации в A-сайт рибосомы заходит второй комплекс aa-тРНК. Это будет та тРНК, чей антикодон комплементарен следующему (за стартовым AUG) кодону.
A(аминоацил)- и P(пептидил)-сайты располагают комплексы аа-тРНК так, что между аминокислотами протекает химическая реакция, и образуется пептидная связь.
После этого первая (находящаяся в P-сайте) тРНК освобождается от своей аминокислоты. В результате последняя оказывается связанной только со второй аминокислотой пептидной связью. Вторая аминокислота связана со второй тРНК, находящейся в A-сайте.
Рибосома перемещается по нити мРНК на один триплет. При этом первая т-РНК оказывается в E-сайте (exit) рибосомы, после чего покидает ее. Вторая т-РНК, связанная с двумя аминокислотами, переходит в P-сайт. A-сайт освобождается для поступления третьего комплекса аа-тРНК.
Следующие циклы элонгации протекают аналогично первому. Когда A-сайт освобождается, в него может зайти аа-тРНК, чей антикодон комплементарен кодону мРНК, находящемся в этот момент в A-сайте.
Терминация трансляции
Терминация — это завершения синтеза полипептидной цепочки и ее отделение. Терминация наступает, когда рибосома встречает один из терминирующих кодонов (UAA, UAG, UGA), для которых не существует своих тРНК. Эти участки мРНК распознаются специальными белками — факторами терминации.
plustilino © 2019. All Rights Reserved

 Пептидная связь: образование, строение …
Пептидная связь: образование, строение … 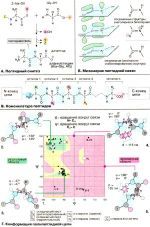 Пептидная связь
Пептидная связь  Аминокислоты. Пептиды. Белки …
Аминокислоты. Пептиды. Белки …